
- Szerző Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Utoljára módosítva 2025-01-22 16:59.
Korlátozás nak,-nek Dalton törvénye
Az törvény alacsony nyomáson jó a valódi gázokhoz, de nagy nyomáson jelentősen eltér. A gázkeverék természeténél fogva nem reakcióképes. Azt is feltételezzük, hogy az egyes gázok molekulái közötti kölcsönhatás megegyezik a keverék molekuláival.
Ilyen módon mit mond ki Dalton törvénye?
A kémiában és a fizikában Dalton törvénye (más néven Dalton törvénye részleges nyomás) Államok hogy nem reagáló gázok keverékében a kifejtett össznyomás van egyenlő az egyes gázok parciális nyomásainak összegével.
A fentieken kívül miért fontos a Dalton-törvény? Dalton törvénye különösen az fontos légköri tanulmányokban. A légkör főként nitrogénből, oxigénből, szén-dioxidból és vízgőzökből áll; a teljes légköri nyomás az egyes gázok parciális nyomásának összege. Dalton törvénye nagy szerepet játszik az orvostudományban és más légzési területeken.
Akkor mi marad állandó Dalton törvényében?
Ismét a gázok kinetikai elmélete és az ideális gáz alapján törvény , Dalton törvénye a mólszámra is alkalmazható úgy, hogy a teljes mólszám egyenlő az egyes gázok mólszámának összegével. Itt tartják a nyomást, a hőmérsékletet és a térfogatot állandó a rendszerben.
Hogyan fedezte fel Dalton a parciális nyomás törvényét?
Dalton törvénye Dalton törvénye gázokon végzett kísérletek vezettek felfedezéséhez, hogy a teljes nyomás gázkeverékének összege a részleges nyomások hogy minden egyes gáz ugyanazt a teret elfoglalva fejtette ki. 1803-ban ez a tudományos elv hivatalosan is ismertté vált Dalton parciális nyomások törvénye.
Ajánlott:
Mit jelent a sűrűségfüggő korlátozó tényező?
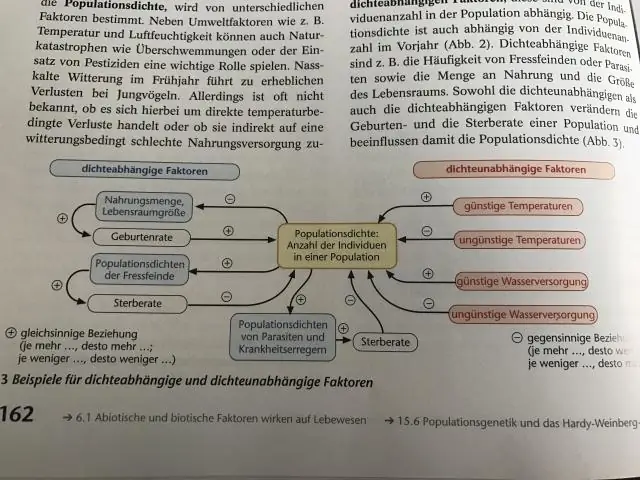
Sűrűségfüggő korlátozó tényezők A sűrűségfüggő tényezők olyan tényezők, amelyeknek a népesség méretére vagy növekedésére gyakorolt hatása a népsűrűség függvényében változik. Sokféle sűrűségfüggő korlátozó tényező létezik, mint pl. a táplálék elérhetősége, a ragadozás, a betegségek és a migráció
Mi a kétféle korlátozó tényező?

A korlátozó tényezők további kategóriákra is feloszthatók. A fizikai vagy abiotikus tényezők közé tartozik a hőmérséklet, a víz elérhetősége, az oxigén, a sótartalom, a fény, az élelmiszer és a tápanyagok; biológiai tényezők vagy biotikus tényezők, olyan organizmusok közötti kölcsönhatásokat foglalnak magukban, mint a ragadozás, a versengés, a parazitizmus és a növényevő
Mit jelent korlátozó tényező?

A korlátozó tényező meghatározása. 1: az a tényező, amely korlátozza a reakciósebességet bármely fiziológiai folyamatban, amelyet sok változó szabályoz. 2: az a környezeti tényező, amely túlnyomó jelentőségű a populáció méretének korlátozásában, a téli böngészés hiánya számos szarvascsorda számára korlátozó tényező
Amikor az élőlények korlátozó tényezőkkel szembesülnek, milyen típusú növekedést mutatnak?

Ha az élőlények korlátozó tényezőkkel szembesülnek, logisztikus növekedést mutatnak (S-alakú görbe, B görbe: az alábbi ábra). Az olyan erőforrásokért folyó verseny, mint az élelmiszer és az űr, a növekedési ütem leáll, így a népesség kiegyenlítődik. Ez a lapos felső vonal a növekedési görbén a teherbírást jelenti
Mi a korlátozó reagens képlete?

Keresse meg a korlátozó reagenst az egyes reagensek mólszámának megtekintésével. Határozza meg a kémiai reakció kiegyensúlyozott kémiai egyenletét! Konvertálja az összes megadott információt anyajegyekké (valószínűleg a moláris tömeg konverziós tényezőként való használatával). Számítsa ki a mólarányt a megadott információkból
