
Tartalomjegyzék:
- Szerző Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Utoljára módosítva 2025-01-22 17:00.
Puffer
- Ha csak gyenge sav . Határozza meg a koncentrációját sav (feltételezve, hogy nincs disszociáció). Nézz fel vagy határozd meg Ka.
- Ha van egy gyenge sav ÉS a konjugátum bázis . Oldja meg a pufferért.
- Ha csak a konjugátum van meg bázis . Oldja meg a pH-ért bázis K segítségévelb és a hidrolízis egyenlet.
Ennek megfelelően hogyan kell savbázis titrálást végezni?
Titrálási eljárás
- Öblítse le a bürettát a standard oldattal, a pipettát az ismeretlen oldattal, az Erlenmeyer-lombikot pedig desztillált vízzel.
- Helyezzen egy pontosan kimért térfogatú analitot az Erlenmeyer-lombikba pipettával, néhány csepp indikátorral együtt.
Hasonlóképpen, hogyan kell kiszámítani a titrálást? Használja a titrálási képlet . Ha a titrálószer és az analit mólaránya 1:1, a képlet van molaritás (M) sav x sav térfogata (V) = molaritás (M) az alap x térfogata (V). ( Molaritás az a koncentráció az oldat egy literenkénti oldott anyag móljainak számával kifejezve.)
Különben is, az F erős vagy gyenge bázis?
Ezért I- a legstabilabb, és a legkevésbé alapvető F - legkevésbé stabil és legalapvetőbb. Erős alapok teljesen kölcsönhatásba lépni erős savak, például a HCl, hogy sót és vizet képezzenek a semlegesítési reakcióban. Egyéb erős alapok oldható oxidok, mint például a Na2O és oldható hidroxid sók. Erős alapok vannak erős elektrolitok.
Mire használják a titrálást?
A titrálás olyan technika, ahol ismert koncentrációjú oldat szokott meghatározza egy ismeretlen oldat koncentrációját. Jellemzően a titrálószert (az ismert oldatot) egy büretából adjuk ismert mennyiségű analithoz (az ismeretlen oldathoz), amíg a reakció befejeződik.
Ajánlott:
Melyek a jelátviteli útvonal lépései?
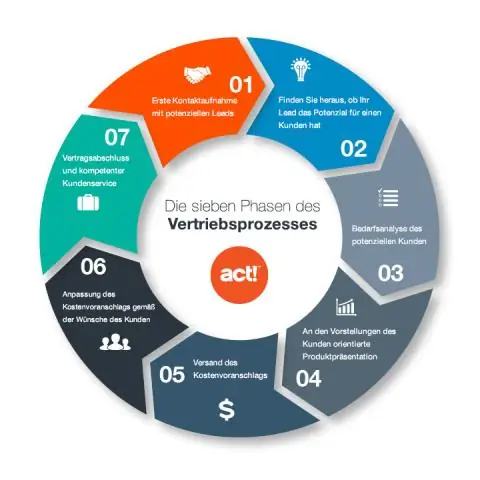
A cellajelzés három szakasza A cellajelzés 3 szakaszra osztható. Recepció: A sejt a sejten kívülről érzékel egy jelzőmolekulát. Transzdukció: Amikor a jelátviteli molekula megköti a receptort, akkor valamilyen módon megváltoztatja a receptor fehérjét. Válasz: Végül a jel egy adott sejtválaszt vált ki
Melyek az erózió lépései?

A víz- és szélerózióban egyaránt közös három lépés: Talajrészecskék LESZÁVOLÍTÁSA: Ez a művelet az eső vagy a szél becsapódási energiája által kiszorítja a részecskéket a talajból. Részecskék SZÁLLÍTÁSA: Ez a művelet talajrészecskéket szállít a mozgó szélben vagy vízben. Részecskék lerakódása új helyen:
Melyek a fő környezetvédelmi problémák Kanadában?

Kanadában sokféle környezeti probléma létezik, beleértve a levegő- és vízszennyezést, az éghajlatváltozást, a bányászatot és a fakitermelést. Ezek a tényezők nem csak Kanadában találhatók meg, hanem szerte a világon
Melyek a szöveges feladatok megoldásának lépései?
Egyszerű lépések a szöveges feladatok megoldásához Olvassa el a feladatot. Kezdje azzal, hogy figyelmesen olvassa el a problémát. Határozza meg és sorolja fel a tényeket. Találja ki, hogy pontosan mit akar a probléma. Távolítsa el a felesleges információkat. Ügyeljen a mértékegységekre. Rajzolj diagramot. Keressen vagy dolgozzon ki egy képletet. Forduljon referenciához
Melyek az egyenlet megoldásának lépései?

Egy kétlépcsős algebrai egyenlet megoldásához mindössze annyit kell tennie, hogy elkülöníti a változót összeadás, kivonás, szorzás vagy osztás segítségével. Oldjon meg egy kétlépcsős egyenletet úgy, hogy osztás helyett a végén szoroz. x/5 + 7 = -3 = (x/5 + 7) - 7 = -3 - 7 = x/5 = -10. x/5 * 5 = -10 * 5. x = -50
