
- Szerző Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Utoljára módosítva 2025-01-22 16:59.
A klór izotóp A 18 neutronból álló vegyület abundanciája 0,7577, tömegszáma pedig 35 amu. Kiszámításához a átlagos atomtömeg, szorozd meg a törtet a tömegszámmal mindegyik esetében izotóp , majd add össze őket.
Hasonlóképpen, mennyi egy elem összes izotópjának súlyozott átlaga?
A különböző tömegek felhasználásával izotópok és mindegyik milyen bőséges izotóp azaz megtalálhatjuk a átlagos an atomjainak tömege elem . Az atomtömeg egy elem az a súlyozott átlag az atomok tömege a természetben előforduló mintában elem . Az atomtömeget általában atomtömeg-egységekben adják meg.
minek a tömege 1 amu? Az atomtömeg-egységet (az AMU-t vagy amu-t szimbolizáljuk) úgy definiáljuk, mint egy 12 szénatom tömegének pontosan 1/12-ét. A szén-12 (C-12) atom hat protonok és hat neutronok magjában. Pontatlan kifejezésekkel egy AMU az átlaga proton nyugalmi tömeg és a neutron pihenő tömeg.
Másodszor, hogyan számítja ki a százalékos bőséget az atomtömeg segítségével?
Változtassa meg mindegyiket százalékos bőség decimális formába osztva 100-zal. Ezt az értéket szorozzuk meg a atomtömeg annak az izotópnak. Adja össze az egyes izotópokat, hogy megkapja az átlagot atomtömeg.
Mi a különbség az atomtömeg és az atomtömeg között?
Atomtömeg (ma) az a tömeg Egy atom . Egyetlen atom meghatározott számú protonnal és neutronnal rendelkezik, így a tömeg egyértelmű (nem fog változni), és a protonok és neutronok számának összege az atomban . Atomtömeg súlyozott átlaga a tömeg az összes közül atomok az izotópok bősége alapján.
Ajánlott:
Hogyan lehet megtalálni egy elem elektronhéját?

Minden héj csak meghatározott számú elektront tartalmazhat: Az első héj legfeljebb két elektront, a második legfeljebb nyolc (2 + 6) elektront, a harmadik héj legfeljebb 18 (2 + 6 + 10) elektront tartalmazhat. ) stb. Az általános képlet az, hogy az n-edik héj elvileg legfeljebb 2(n2) elektront tud tartani
Hogyan lehet megtalálni egy derékszögű háromszög átlóját?

Egy derékszögű háromszög átlójának (orhipoténuszának) hosszának meghatározásához helyettesítse be a két merőleges oldal hosszát az a2 +b2 = c2 képletbe, ahol a és b a merőleges oldalak hossza, c pedig a hipoténusz hossza
Hogyan lehet súlyozott átlagot létrehozni egy kimutatástáblázatban?

Súlyozott átlagok a kimutatásban Kattintson a kimutatás szó melletti lefelé mutató nyílra a kimutatás eszköztár bal oldalán. Válassza a Képletek | Számított mezők. A Név mezőben adja meg az új mező nevét. A Képlet mezőbe írja be a súlyozott átlaghoz használni kívánt képletet, például =WeightedValue/Weight. Kattintson az OK gombra
Hogyan lehet megtalálni az egy pontra merőleges egyenes egyenletét?
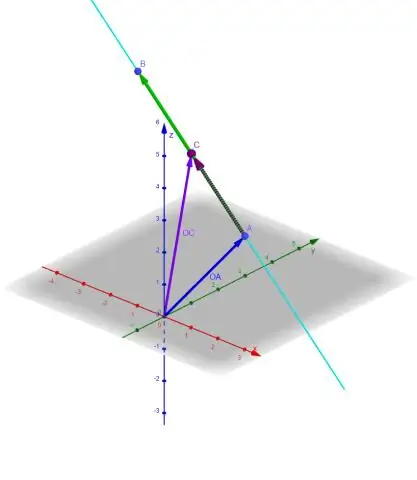
Először tedd a megadott egyenes egyenletét lejtőmetszet alakba úgy, hogy megoldod y-t. y = 2x +5, tehát a meredekség –2. A merőleges egyeneseknek ellentétes-reciprok meredeksége van, így a keresett egyenes meredeksége 1/2. Az y = 1/2x + b egyenletbe adott pontot bedugva és b-re megoldva b =6-ot kapunk
Hogyan lehet megtalálni egy kocka térfogatát, amelynek tetején piramis van?
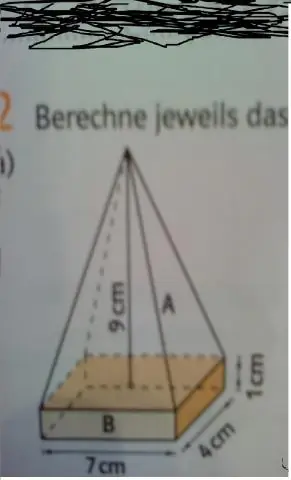
A kocka térfogatának meghatározásához szorozza meg az alapot a szélesség és a magasság szorzatával. A piramis térfogatának meghatározásához vegye az alap területét, egin{align*}Bend{align*}, és szorozza meg a magasság szorzatával, majd szorozza meg egin{align*}frac{1}{3}end{ igazítsa*}
